

г. Киев, Симона Петлюри, 28

+38 (096) 515 79 79
+38 (093) 414 79 79
13 мая. 2020
Все Новости
По данным экспертов ВОЗ, основанным на последних результатах эпидемиологических исследований, интактный пародонт встречался лишь в 2-10 % наблюдений, заболевания пародонта отмечаются у 90-95 % взрослого населения. Увеличение распространенности генерализованных заболеваний тканей пародонта приходится в основном на возраст от 30 до 50 лет, и к 45 годам достигает 96 %. Среди молодежи в возрасте от 16 до 20 лет распространенность заболеваний тканей пародонта резко увеличивается и встречается в 50-85 %.
Повышенная распространенность генерализованных заболеваний тканей пародонта, характеризующихся длительным хроническим течением, со склонностью к периодическому обострению с последующим прогрессированием воспалительно-дистрофического процесса, который приводит к развитию структурных и функциональных нарушений зубочелюстного аппарата, является одной из основных медико-социальных проблем.
В этой связи разработка новых подходов к лечению ГП, направленных на достижение долговременной стабилизации в течении ГП, занимает одно из приоритетных направлений в развитии современной стоматологии
Исследования последних лет позволили существенно углубить представление о механизмах возникновения и прогрессирования хронических дистрофически-воспалительных заболеваний пародонта. Согласно современным представлениям этиологические факторы ГП традиционно подразделяются на местные и системные. К местным относятся факторы, которые действуют непосредственно на ткани пародонта, тогда как системные зависят от общего состояния больного
Среди наиболее значимых этиологических факторов развития ГП исследователи выделяют влияние пародонтопатогенных микроорганизмов и продуктов их жизнедеятельности на ткани пародонта, на состояние полости рта, что способствует образованию зубной бляшки и влияет на пародонтопатогенный потенциал микрофлоры, общие (системные) факторы, обеспечивающие гомеостаз пародонта на фоне имеющейся генетической предрасположенности, изменения реактивности организма. Среди важных факторов риска развития ГП также называют нарушение микроциркуляции и транскапилярного обмена, дисбаланс иммунокомпетентных систем, привлечение аутоиммунитета, недостаточность антиоксидантной защиты.
Согласно «сосудистой теории» патогенеза ГП — микроциркуляторные расстройства появляются уже на ранних стадиях ГП и сопровождают все периоды заболевания. Они характеризуются торможением скорости кровотока, агрегацией и стазом форменных элементов крови, повреждением эндотелиальных клеток, что способствует тромбообразованию.
Высокая распространенность заболеваний, сопровождающихся дисфункцией эндотелия (ЭД), прежде всего атеросклероза, способствует развитию дисбаланса между механизмами антиоксидантной защиты и скоростью СРО. Перекисное окисление фосфолипидов клеточных мембран способствует их деструкции, повреждению клеток пародонта, что в свою очередь снижает устойчивость тканей к повреждающим этиологическим факторам, в т. ч. и микробного воздействия.
Накопление недоокисленных продуктов способствует и изменениям в костной ткани альвеолярного отростка с активацией процессов резорбции кости и деструкции коллагеновых волокон. Активация СРО сопровождается изменением рН клеток эндотелия сосудов, тканей пародонта с развитием метаболического ацидоза и изменений свойств клеточных мембран . Современные представления о роли оксидативного стресса в патогенезе хронического пародонтита позволяют рассматривать содержание переокисленных липидов в слюне и ее антиокислительный потенциал в качестве предикторов эскалации воспалительного поражения пародонта.
Таким образом, возникновению функциональных и морфологических изменений в тканях пародонта способствуют универсальные патогенетические механизмы, формирующиеся при различных заболеваниях органов и систем.
Поэтому при лечении становится актуальной клеточная инженерия, базирующаяся на использовании для активации процессов репаративной регенерации тканевых структур факторов роста, которые продуцируют многие клетки, например, тромбоциты.
Еще в 1990-х гг. было доказано, что в тромбоцитах нашей крови имеются факторы роста – белки, которые стимулируют развитие стволовых клеток и превращение их в клетки той ткани организма, которая повреждена.
Терапевтический эффект тромбоцитарной аутоплазмы (ТАП) объясняется присутствием тромбоцитов и содержащихся в них факторов роста (ФР), но эффект плазмы крови может быть основан и на других качественных составляющих, например микро- и макроэлементах, витаминах, находящихся в наиболее биодоступном для тканей состоянии.
В настоящее время основной целью исследований процессов регенерации является необходимость идентификации ФР, знания механизма их действия и возможностей применения для улучшения регенерации раневой поверхности.
Использование ТАП сегодня представляет одну из немногих возможностей запускать и ускорять естественные механизмы регенерации за счет содержащихся в тромбоцитах ФР. Кроме того, она не токсична и не иммунореактивна. Получение ТАП подразумевает разделение плазмы и тромбоцитов от эритроцитов как по градиенту плотности, так и с использованием специализированных лабораторных фильтров.
ТАП модулирует и регулирует функцию первичных, вторичных и третичных ФР, влияя на все стадии регенерации одновременно. Упомянутое свойство отличает ФР тромбоцитарной аутоплазмы от рекомбинантных ФР, отвечающих за отдельный механизм регенерации.
Тромбоциты в своем составе имеют разнообразные ФР и цитокины, которые способствуют восстановлению поврежденных тканей. В α-гранулах тромбоцитов находятся свыше 30 ФР, которые влияют на процессы регенерации тканей пародонта одновременно. Наибольшее значение имеют: IGF (инсулиноподобный ФР) – способствует дифференцированию стволовых клеток, увеличивает метаболизм костной ткани и продуцирование коллагена. PDGF (тромбоцитарный ФР) – стимулирует пролиферацию и перемещение мезенхимальных (остеогенных) клеток, стимулирует ангиогенез. PDEGF (тромбоцитарный ФР эндотелиальных клеток) – вызывает стимулирующее действие на эндотелиальные клетки и обладает ангиогенным эффектом. VEGF или PDAF (ФР эндотелия сосудов) – имеются 4 вида фактора VEGF-A, -B, -C и -D. Участвуют в ангиогенезе, индуцируют пролиферацию эндотелиальных клеток сосудов. EGF (эпидермальный ФР) – способствует пролиферации фибро- и остеобластов, увеличивает синтез фибронектина. TGF-ß («Семейство» трансформирующего ФР) – многофункциональные факторы, т. к. не только индуцируют дифференцирование мезенхимальных клеток, а также вызывают большое количество клеточных и межклеточных ответов, включая продукцию других ФР. К трансформирующим ФР относятся костные морфогенетические белки, часть которых (КМБ-2, остеогенин или КМБ-3, КМБ-4, -5, -7, -8 и -9) являются выраженными остеоиндукторами, модулируют клеточную пролиферацию и дифференцировку малодифференцированных клеток в остеобласты. PLGF-1/-2 (плацентарные ФР) – потенцируют действие VEGF, повышают проницаемость сосудистой стенки. FGF (фибробластный ФР) – вызывает экспрессию в костной ткани, ангиогенез, оссификацию, индуцирует продукцию TGF в остеобластных клетках. Остеонектин – «культуральный шоковый протеин»: составляет 15 % органического компонента костного матрикса, регулирует пролиферацию и взаимодействие клеток с матриксом. Тромбоспондин – опосредует адгезию костных клеток. ФР доставляются в ткани при инъекционной форме аутоплазмы и концентрируются при помощи введения большего количества аутоплазмы – это повышает активность фибробластов и стимулирует их образование. Фибробласты продуцируют коллагеновые волокна, гиалуроновую кислоту и эластин. Все это приводит к образованию новой соединительной ткани, росту капилляров. ФР также блокируют остеокласты и стимулируют пролиферацию остеобластов, что сдерживает дальнейшую убыль костной ткани и способствует ее регенерации. В итоге восстанавливаются обменные процессы, улучшаются микроциркуляция и метаболизм в клетках тканей, нормализуется тканевое дыхание, активизируется местный иммунитет.
Противопоказаниями к использованию метода являются: злокачественные новообразования; системные заболевания крови, психические заболевания, аллергическая реакция на антикоагулянт (натрий-гепарин) в анамнезе.
Для лечения пациентов используется аутоплазма полученная по следующим методикам.

1) Получение обогащённой тромбоцитами плазмы PRP (Platelets Reach Plasma, Lifting-Plasma), которая в дальнейшем НЕ загустеет. Для использования PRP-плазмы используют антикоагулянт. Её используют для PRP-терапии. Методика получения PRP предполагает, что плазма не свернётся ни до введения в организм пациента, ни после. Механизм действия — всё те же факторы роста.
В пробирках для получения формы PRP — Platelet rich plasma мы используем антикоагулянт ACD — A. Выбор антикоагулянта не случаен. Именно этот антикоагулянт позволяет обеспечить максимальную выживаемость и активность тромбоцитов. В банках крови именно это антикоагулянт используется для хранения тромбоцитарной массы. При однократном центрифугировании в пробирке мы видим разделение на эритроцитарно-лейкоцитарный слой (темный) и плазму. Иногда между ними есть ярко выраженный белесый слой, он называется Buffy Coat — это фракция антикоагулированного образца крови, которая содержит большинство лейкоцитов и тромбоцитов после центрифугирования в градиенте плотности крови.
2) PRF (Platelets Reach Fibrin) – богатый тромбоцитами фибрин, антикоагулянт не используется:
а) A-PRF (advance, то есть «улучшенный», PRF-сгустки) — получение обогащённой тромбоцитами плазмы, которая загустеет до применения (антикоагулянт не используется). Это загустевшая часть плазмы крови, содержащая много факторов роста для остео- и ангиогенеза. Из них можно приготовить мембраны и пробки с помощью специального бокса PRF-BOX. Суть PRF-BOX в отжатии фибрина с целью его освобождения от лишней плазмы. Мембранами укрывают костные материалы, дефекты неба после забора десневых трансплантатов, мембрану Шнайдера при её перфорациях и просто синус-лифтах, используют для хирургии пародонта. Пробки — для заполнения постэкстракционных лунок зубов и пародонтальных дефектов. Так же, сгустки можно нарезать ножницами на мелкие кусочки и смешивать их с костными заменителями.
б) i-PRF (injectable – инъекционный) – получение обогащённой тромбоцитами плазмы, которая загустеет после применения. Такую плазму используют для смешивания с костным заменителем, с целью его стабилизации и придания ему определенной формы. Для инъекций в пародонтальные ткани c целью улучшения их кровоснабжения, изменения биотипа десны. Иногда для склеивания краев слизистой оболочки, например, мембраны Шнайдера.
Для получения PRF необходимое количество крови быстро забирается в пробирки без антикоагулянта и сразу же центрифугируется и после центрифугирования у нас есть 8-12 минут для инъекций, потому что отсутствие антикоагулянта приводит к неминуемому свертыванию полученной плазмы и самое прекрасное, если мы введем плазму в жидком виде, а процесс свертывания завершиться в тканях, формируя естественную матрицу для клеточного восстановления тканей
Активация тромбоцитов в ответ на повреждение тканей происходит во время процесса высвобождения PRF нескольких биологически активных белков, в том числе; альфа-гранулы тромбоцитов, фактор роста, полученный из тромбоцитов (PGDF), трансформирующие факторы роста-β (TGF-β), сосудистый эндотелиальный фактор роста (VEGF) и эпидермальный фактор роста. На самом деле цитокины тромбоцитов и лейкоцитов играют важную роль в ролевой игре этого биоматериала, но поддерживающий их фибриновый матрикс очень полезен для формирования определяющих элементов, отвечающих за реальный терапевтический потенциал PRF. Цитокины немедленно используются и разрушаются в заживающей ране. Гармония между цитокинами и поддерживающей их фибриновой матрицей имеет гораздо более уникальное значение, чем любое другое производное тромбоцитов.
3) PPP – Platelet Poor Plasma — тромбоцитами плазма с концентрацией тромбоцитов «Norma». В пробирках с зеленым стикером исходно есть разделительный гель. Это удобно, потому что гель после центрифугирования поднимается и плотно фиксирует эритроцитарно-лейкоцитарный сгусток, препятствуя смешиванию с плазмой, НО параметры центрифугирования для пробирок содержащих гель не позволяют применить низкие скорости центрифугирования и в связи с этим конечный продукт, плазма, не может содержать высокие концентрации тромбоцитов, однако содержание белков, аминокислот, минералов и всего остального остается неизменным, что дает нам возможность применять эту форму практически везде, так как она восстанавливает все нарушенные функции тканей.
Сегодня существует широкий арсенал методов и средств, разработанных для комплексного лечения генерализованного пародонтита и хронического катарального гингивита, при этом достичь устойчивой стабилизации патологического процесса в тканях пародонта сложно. Вопрос определения оптимального подхода к лечению данной категории больных является весьма актуальным и требует проведения дальнейших исследований. Лечение заболеваний пародонта важно не только для поддержания здоровья полости рта, но, как показывает анализ литературных источников, и для снижения патологических изменений в тканях пародонта, что даст возможность разработать новый комплексный патогенетически обоснованный подход к лечению генерализованного пародонтита и хронического катарального гингивита, направленный на стойкую стабилизацию дистрофически-воспалительного процесса в тканях пародонта, который одновременно будет способствовать укреплению здоровья пациентов в целом.
В исследовании принимали участия 27 человек, из них 13 мужчина и 14 женщин в возрасте от 25 до 65 лет, с диагнозами: хронический катаральный гингивит средней степени тяжести, хронический генерализованный пародонтит начальной-I и II степени тяжести. Все пациенты были разделены на 2 группы: контрольная – 12 человек и основная — 15 пациентов. Лечение гингивита и пародонтита включало в себя лечение кариеса и его осложнений; обучение пациентов гигиене полости рта и ее контроль; проведение профессиональной гигиены и закрытого кюретажа. Общая противовоспалительная терапия назначалась пациентам с диагнозом генерализованный пародонтит и проводилась с использованием антибактериальных препаратов. Традиционная терапия дополнялась назначением Биогая Продентис, рассасывать 3-4 раза в день в течении 10 дней. В основной группе: при гингивите и начальной-I степени пародонтита после профессиональной гигиены, при пародонтите — после закрытого кюретажа, — применялось введение iPRF в область переходной складки. Всего проводили 3 процедуры с интервалом 10 дней, последующие 2 процедуры вводили — PPP. Оценка результатов: после каждой процедуры – контрольный осмотр; следующий визит – через 6 месяцев. Если необходимо через 6 месяцев проводили поддерживающую терапию – курс профессиональной гигиены с 1 процедурой PPP (если необходимо).

Фото 1. Пациентка М., 28 лет. Диагноз: хронический катаральный гингивит средней степени тяжести. До лечения.

Фото 2. Пациентка М., 28 лет. Диагноз: хронический катаральный гингивит средней степени тяжести. Сразу после лечения: снятие зубных отложений и первой процедуры плазмотерапии – iPRF.
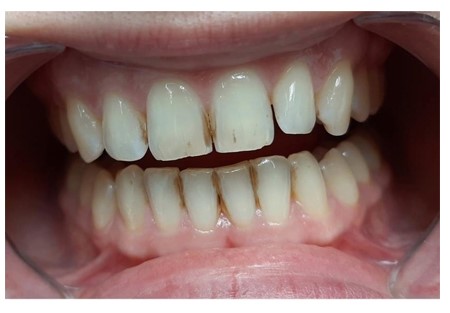
Фото 3. Пациентка М., 28 лет. Диагноз: хронический катаральный гингивит средней степени тяжести. Спустя 3 года после лечения.

Фото 4. Пациент 32 года. Генерализованый пародонтит лёгкой степени тяжести. Зубные отложения. До лечения

Фото 5.Пациент 32 года. Генерализованый пародонтит лёгкой степени тяжести. Зубные отложения. Сразу после скейлинга и инъекций I-PRF.

Фото 6. Пациент 32 года. Генерализованый пародонтит лёгкой степени тяжести. Зубные отложения. Спустя 5 дней после лечения.
Уже через неделю от начала лечения у пациентов основной группы, которым проводили инъекции тромбоцитарной аутоплазмы, отмечалась положительная клиническая динамика, которая выражалась в улучшении показателей гигиенического и пародонтальных индексов на 40 %, в снижении кровоточивости десен на 60 %, уменьшении гиперемии десен. В контрольной группе больных в 70 % случаев в этот срок сохранялись жалобы на кровоточивость десен, ограниченную гиперемию папиллярной десны. Индексные показатели не отличались от исходного уровня.
Через 6 месяцев после проведенного лечения пациентов II (основной) группы признаки воспаления пародонта купировались полностью: отсутствовала кровоточивость, отек, гиперемия десны, уменьшилась глубина зондирования пародонтальных карманов. В контрольной группе больных кровоточивость десен снизилась на 50 % по сравнению с исходными значениями. Отечность папиллярного края десны и глубина пародонтальных карманов оставались на исходном уровне.
Через 12 месяцев у пациентов основной группы клиническое состояние пародонта было стабильным, что подтверждалось отсутствием прироста показателей пародонтальных индексов, восстановлением функции зубов. В контрольной группе индексные значения, характеризующие состояние пародонта, оставались в 2,5 раза более высокими, чем в группе сравнения.
Результаты исследования показали эффективность и, соответственно, обоснованность применения тромбоцитарной аутоплазмы в комплексном лечении заболеваний пародонта. Снижение индексных значений, характеризующих состояние пародонта, во II группе пациентов отмечалось уже к 7 суткам от начала лечения. Аналогичные показатели в контрольной группе в этот срок практически не отличались от исходных. Через 12 месяцев после лечения снижение (нормализация) пародонтальных индексов во II группе произошло на 82 %, а в I (контрольной) – всего на 65 %.
Заключение. Включение тромбоцитарной аутоплазмы в комплексное лечение пародонтита позволяет купировать воспаление и стабилизировать процесс в более короткие сроки по сравнению с общепринятыми методами лечения.